Une existence prouvée mais pas officialisée, telle était le statut de l'espèce « Botrytis groupe I » en 2006. Bien que révélée, cette nouvelle espèce de Botrytis, différente de Botrytis cinerea au sens strict, n'avait jamais été caractérisée de manière formelle.
Ce travail vise à établir définitivement le groupe I de Botrytis comme nouvelle espèce, en utilisant les critères cités dans l'encadré 1. Le nom proposé est B. pseudocinerea (tel. Botryotinia pseudofuckeliana).
Des souches et des critères
Souches de collection et collecte en Champagne
Nous avons analysé des souches pures du genre Botrytis issues des collections de l'INRA Bioger ou de collections internationales. Ces souches ont servi pour la caractérisation fine utilisant les 4 critères d'espèce définis dans l'encadré 1.
Nous avons également collecté 1 088 souches champenoises, soit sur vigne, soit sur ronce, entre l'automne 2005 et le printemps 2007 (4 dates de collecte) des populations de Botrytis sp., afin d'estimer la structure des populations naturelles.
Critère phylogénétique : trois gènes séquencés, arbre établi
Nous avons actualisé la phylogénie du genre Botrytis, en intégrant de nouvelles souches du groupe II et des souches du groupe I dans celle préalablement établie (Staats et al., 2005).
Nous avons séquencé 3 gènes choisis comme bons marqueurs phylogénétiques (G3PDH, HSP60, MS47) puis établi un arbre phylogénétique pour chaque gène selon la méthode du maximum de vraisemblance.
Nous avons ensuite comparé la topologie de ces arbres pour vérifier leur congruence (indice Icong) puis nous avons établi un arbre consensus en concaténant les séquences individuelles des trois gènes.
Nous avons enfin testé une horloge moléculaire afin d'estimer le temps de divergence entre les espèces des groupes I et II.
Critère biologique : croisements mais aussi profils alléliques
Après avoir déterminé leur type sexuel, nous avons réalisé des croisements inter et intragroupes selon une méthode précédemment établie (Faretra et al., 1988). Pour chaque croisement, et après incubation de 4 à 6 mois, nous avons observé la production d'apothécies, organes de la reproduction sexuée chez Botrytis.
Nous avons également étendu ce critère au niveau populationnel, en établissant le profil allélique des 1 088 individus de populations naturelles pour 8 loci microsatellites neutres (Fournier et al., 2002) et en recherchant la présence de l'élément transposable flipper. Nous avons ensuite utilisé une méthode d'assignation (logiciel Structure) afin d'affecter les individus dans des clusters génétiquement stables. Puis nous avons mesuré la diversité génétique dans ces clusters cohabitant dans les populations naturelles de pourriture grise, estimant ainsi les potentialités de recombinaisons génétiques dans la nature.
Critère phénétique : aspects visibles
Nous avons mesuré le diamètre et la surface des conidies (spores asexuées) dans des conditions standardisées de souches des groupes I et II.
Les caractères morphologiques des colonies, du mycélium, des conidies, apothécies et spermaties ont été observés par une spécialiste de la taxonomie des champignons pour établir la diagnose latine nécessaire à l'établissement de toute nouvelle espèce. Enfin, nous avons mesuré en conditions standardisées le taux de germination et la vitesse de croissance sur milieu PDA.
Critère écologique : comportement au champ et en conditions contrôlées
Nous avons noté l'abondance relative des deux espèces au cours du temps, au sein d'une population naturelle, collectée sur matériel soit vivant (baies infectées à l'automne), soit mort (pièces florales sèches au printemps).
De plus, nous avons mesuré la vitesse de croissance sur des milieux synthétiques plus ou moins riches en sucres et à diverses températures (plage allant de 7 °C à 27 °C, pour un optimum connu à 20 °C pour cette espèce).
Nous avons aussi noté la production de sclérotes (forme de conservation du champignon) produits à différentes températures par les souches des deux espèces.
Enfin, nous avons évalué l'agressivité des isolats des deux groupes en les inoculant sur feuilles de haricot et de tomate et en mesurant le diamètre des nécroses générées.
Résultats selon le critère phylogénétique
Deux espèces distinctes
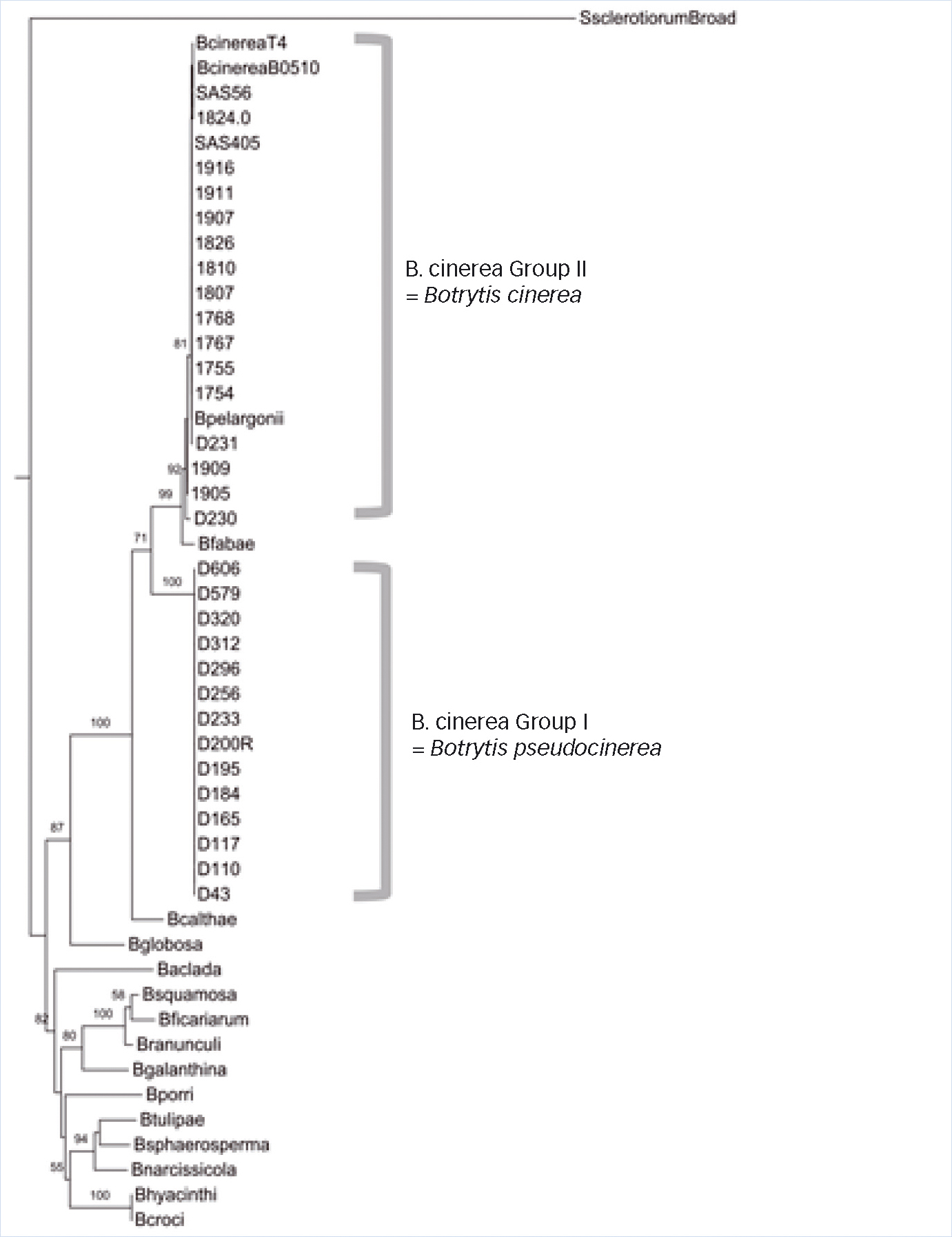
Les arbres individuels construits pour les gènes G3PDH, HSP60 et MS547, ainsi que l'arbre concaténé construit à partir des séquences précédentes, montrent des topologies congruentes, de manière significative [indice Icong ; détails dans (Walker et al., 2011) ; arbre consensus reproduit Figure 2]. Les souches du groupe I forment un clade proche mais distinct de B. cinerea, fortement différentié par une valeur de bootstrap de 100 %, ce qui caractérise en général deux espèces différentes.
Cet arbre a été construit à partir des séquences concaténées obtenues pour les gènes G3PDH, HSP60 et MS547, soit une séquence concaténée de 2 492 paires de bases.
L'arbre consensus a été obtenu grâce à la méthode du maximum de vraisemblance (modèle HKY +I +G). Des permutations aléatoires des branches de l'arbre (100) permettent d'estimer le nombre de fois où une branche considérée est réellement considérée dans l'arbre. Plus cette valeur de bootstrap est forte, plus la structure de l'arbre est solide. La séquence concaténée équivalente de Sclerotinia sclerotiorum (espèce proche de B. cinerea) sert à enraciner l'arbre.
Même pas sœurs !
Fait surprenant, ces deux espèces ne sont pas des espèces sœurs : B. cinerea est plus proche de B. fabae que de Botrytis groupe I.
Les tests statistiques confirment l'hypothèse d'une vitesse d'évolution moléculaire constante sur toutes les branches de l'arbre.
Cette « consultation de l'horloge moléculaire » permet d'estimer un temps de divergence entre les deux espèces de 7 à 18 millions d'années.
Selon le critère biologique
Deux espèces qui ne se croisent pas...
Nous avons réalisé 69 croisements intra et interspécifiques (8 croisements intragroupe II , 50 croisements intra-groupe I et 11 croisements inter-groupes), dont 26 croisements témoins (Walker et al., 2011). Seuls les croisements intra-groupe ont fourni des apothécies matures et viables, i.e. contenant des ascospores issues de la reproduction sexuée et capables de produire des colonies vivantes. Un unique croisement groupe II x groupe I a produit quelques apothécies... mais vides (sans ascospores) et avortées.
Côté flux de gènes
En complément de ces croisements inter-individus, nous avons étendu le critère biologique au niveau populationnel en utilisant des marqueurs microsatellites neutres et des outils de génétique des populations pour estimer les flux de gènes entre les deux groupes. L'analyse par le logiciel Structure (qui assigne sans a priori les individus dans des clusters génétiquement homogènes) a décelé deux clusters. Le cluster I ne contient que des individus du groupe I et le cluster II des individus du groupe II (Figure 3).
Cette assignation stricte en deux clusters indépendants montre bien l'indépendance génétique entre les deux groupes.
Sous-clusters décelés et marqueurs obsolètes
Une analyse du cluster II permet de le subdiviser en deux sous-clusters : II a qui contient principalement des individus collectés sur ronce et II b contenant principalement des individus collectés sur vigne.
Cette seconde subdivision confirme l'adaptation à l'hôte déjà démontrée (Fournier & Giraud, 2008) chez B. cinerea.
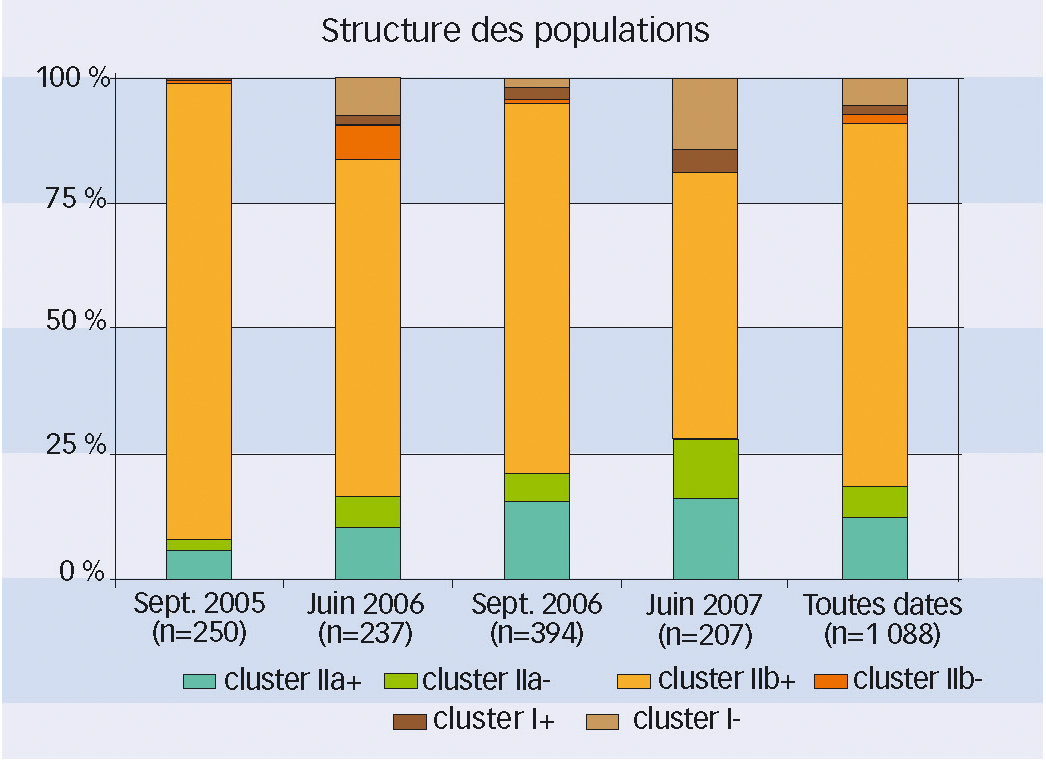
La figure 3 montre l'évolution dans le temps de la taille de chaque cluster (cluster I : souches du groupe I ; cluster II a : souches du groupe II collectées majoritairement sur ronce ; cluster II b : souches du groupe II collectées majoritairement sur vigne). Pour chaque cluster, une couleur différente distingue les souches comportant l'élément transposable flipper (+) ou non (-).
L'espèce groupe I (cluster I) est minoritaire quelle que soit la date de collecte.
L'élément transposable flipper est détecté dans tous les clusters, à fréquence forte pour les clusters II (davantage de II a+ et II b+ que de II a- et II b- respectivement) et faible pour le cluster I (davantage de Ia- que de Ia+).
Ce résultat contredit les observations faites auparavant à partir d'un nombre limité de souches du groupe I, toutes trouvées vacuma. Ainsi, le marqueur vacuma/transposa est obsolète et ne doit plus être utilisé pour caractériser les deux espèces et, plus largement, les populations de pourriture grise.
Des populations génétiquement diversifiées
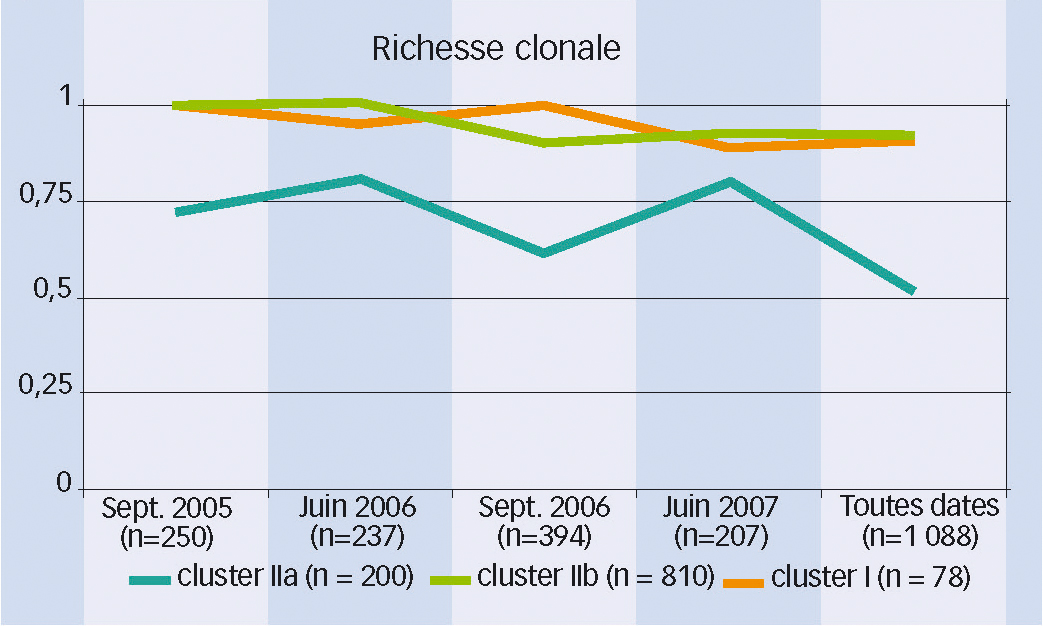
La richesse clonale mesure, dans chaque cluster, la proportion de génotypes multilocus (ou GML = combinaison unique d'allèles aux 8 loci génotypés) distincts par rapport au nombre total d'individus. En d'autres termes, cet indice mesure la proportion de clones différents dans un cluster. Cette proportion est proche de 1 pour les clusters I et II a et de 0,75 pour le cluster II b. Pour ces 3 clusters, la proportion de clones est donc faible (Figure 4).
Ceci indique des populations très diversifiées génétiquement, subissant probablement d'importants flux migratoires ainsi qu'une recombinaison génétique liée à une reproduction sexuée intense. Ainsi, les compartiments hébergeant les espèces des groupes I et II sont donc étanches mais, en revanche, leurs populations ont des comportements similaires.
Selon le critère phénétique
Aspect visuel, pas de différence significative
La mesure du grand diamètre des conidies elliptiques des individus des deux groupes, évaluée en conditions standardisées, ne montre pas de différence significative (12,04 ±1,55 µm pour le groupe I et 11,86 ±1,45 µm pour le groupe II ).
La mesure des surfaces de conidies ne permet pas non plus de distinguer les deux groupes (91,29 ±21,85 µm² pour le groupe I contre 87,77 ±18,84 µm² pour le groupe II ). L'analyse fine des mesures, de la morphologie et de la couleur des différents organes des deux espèces n'a pas montré de différence majeure (Figure 5 page suivante). En revanche, elle a permis d'établir la diagnose latine de la nouvelle espèce B. pseudocinerea. Cette espèce est déposée maintenant officiellement dans une collection internationale (Mycobank ; n° MB 561818).
Sporulation et croissance
Nous n'avons pas observé non plus de différence de taux de sporulation des deux espèces sur milieu PDA solide (en moyenne 96,58 % pour le groupe I et 94,60 % pour le groupe II ).
La vitesse moyenne de croissance sur PDA n'était pas significativement différente entre les deux groupes : 24,10 mm/jour pour le groupe I et 25,56 mm/jour pour le groupe II . Tous ces résultats permettent de conclure qu'il n'existe pas de différence morphologique, pour les critères observés, entre les deux espèces (Walker et al., 2011).
Selon le critère écologique
Groupe I « printanier »
En populations naturelles, les espèces des groupes I et II sont retrouvées au printemps et à l'automne, mais en proportions significativement différentes (Figure 3).
L'espèce du groupe I reste minoritaire, mais à une fréquence plus importante au printemps. Ceci suggère une meilleure adaptation aux conditions climatiques printanières et/ou une meilleure capacité à consommer du matériel végétal mort (capuchons floraux).
Au laboratoire, même agressivité
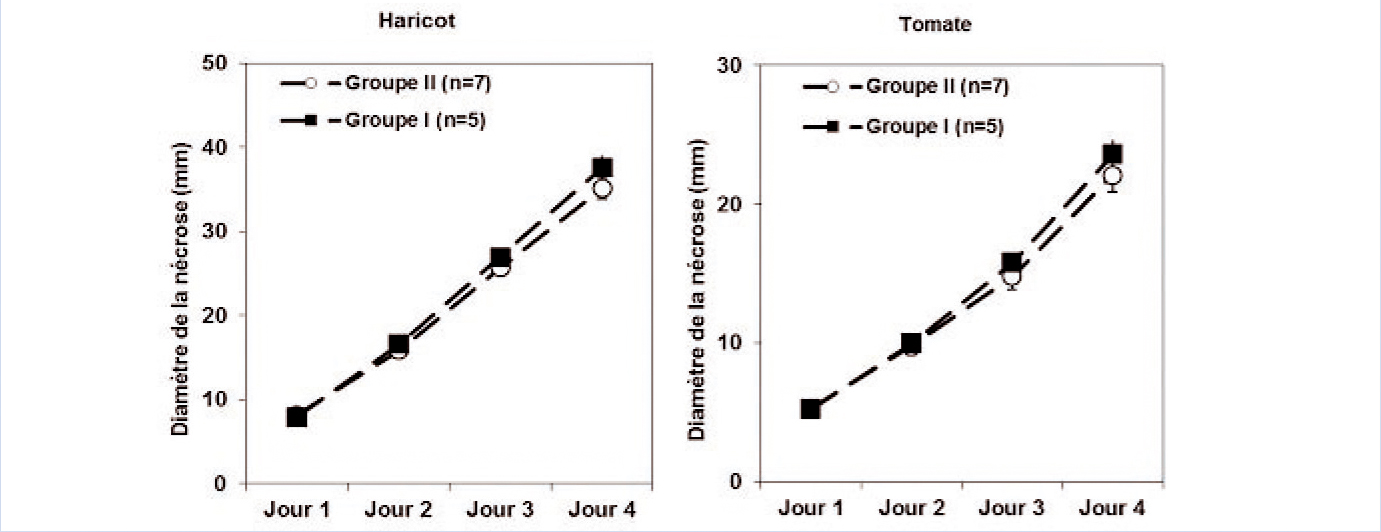
Nous avons donc cherché à préciser ce point en mesurant l'agressivité sur feuilles de tomate ou de haricot détachées et maintenues en survie.
Nous n'avons pas observé de différence significative entre les deux groupes dans leur capacité à produire des lésions sur les feuilles des deux hôtes (Figure 6).
De même, la vitesse de croissance mesurée à une température donnée, et pour un milieu nutritif donné n'était pas significativement différente entre les deux espèces. L'effet de la température et de la richesse du milieu synthétique avaient le même effet significatif sur la croissance des deux espèces (optimum de croissance à 20 °C sur le milieu le plus riche, comme attendu).
De manière similaire, nous n'avons pas observé de variation significative de la production de sclérotes entre les deux espèces (Walker et al., 2011).
Ainsi, les espèces B. cinerea groupe I et II semblent avoir des exigences écologiques distinctes (phénologies différentes), mais nous n'avons pas pu identifier les facteurs responsables de ces adaptations.
Conclusion
Deux espèces dont une nouvellement définie
La pourriture grise de la vigne est causée par un complexe d'au moins deux espèces vivant en sympatrie, B. cinerea (espèce dominante) et B. pseudocinerea (espèce minoritaire nouvellement décrite). Ces deux espèces sont distinguées par :
– leur position différente dans la phylogénie (critère phylogénétique),
– leur incapacité à produire une descendance fertile, avec incapacité des populations respectives à échanger des gènes (critère biologique),
– leurs exigences écologiques, même si les raisons de cette différentiation n'ont pu être mises au clair (critère écologique).
Mais ces deux espèces ne sont, en revanche, pas distingables par leur morphologie (critère phénétique) : il s'agit donc d'espèces cryptiques.
La pratique et la surprise
En pratique, il est peu probable que B. pseudocinerea, de phénologie plutôt printanière et d'abondance faible (fréquence <10 %) participe de façon importante aux dégâts de pourriture grise sur raisin. Ceci facilite la gestion de la maladie au vignoble.
En revanche c'est surprenant car B. pseudocinerea a été décrite comme naturellement résistante au fenhexamid (fongicide de la famille des hydroxyanilides) (Leroux et al., 2002). Ce dernier, appliqué surtout en fin de floraison de la vigne quand l'espèce est abondante, devrait la sélectionner.
Les plus faibles fréquences de cette espèce à la vendange suggèrent que l'optimum écologique de B. pseudocinerea est rencontré au printemps, et que ces souches ont une fitness plus faible à l'automne malgré l'effet du fongicide.
Enfin, si cette résistance naturelle est à ce jour le seul marqueur phénotypique permettant de distinguer les deux espèces, de nombreux marqueurs moléculaires sont disponibles pour discriminer et quantifier les deux espèces dans les populations (Azzedine et al., 2012 ; Leroux et al., 2002).
Remerciements : À Muriel Viaud et Pascal Le Pêcheur pour la fourniture des espèces du genre Botrytis et l'aide apportée pour les tests d'agressivité.
Au CIVC (Comité interprofessionnel des vins de champagne) pour avoir permis l'accès aux populations naturelles.
À Joëlle Dupont (Muséum d'Histoire Naturelle de Paris) et Giuseppe Consiglia (Université de Bologne, Italie) pour l'établissement de la diagnose latine.
1- De l'origine... à la définition... des espèces
Qu'est-ce qu'une espèce ?
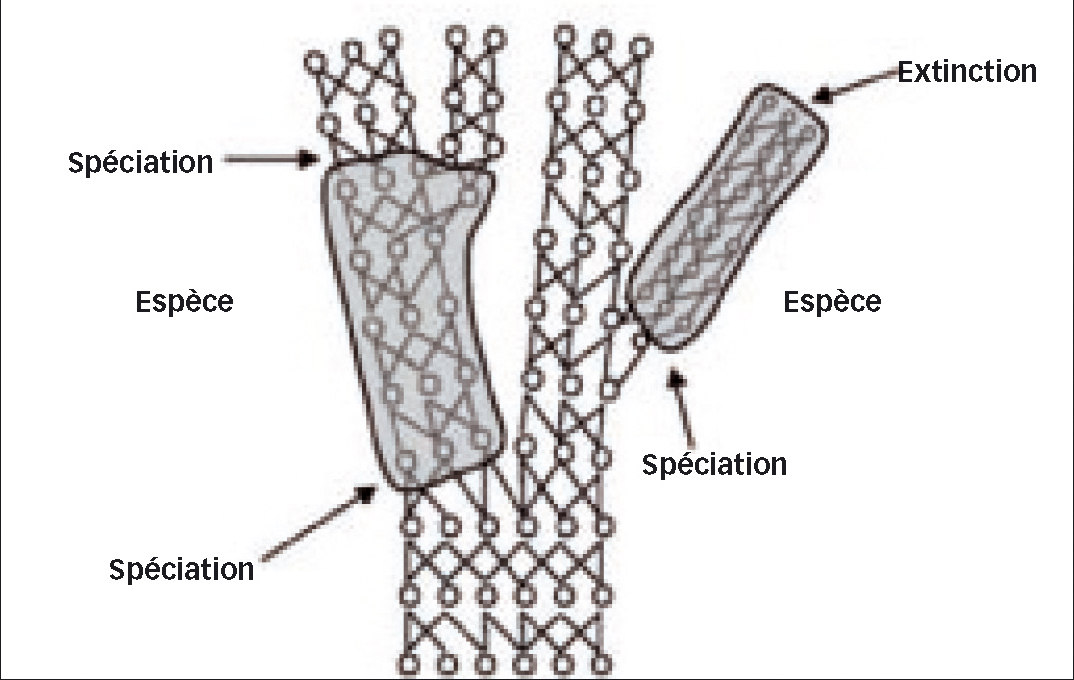
Après large débat, la communauté scientifique a abouti récemment à la définition illustrée figure 1 : « Une espèce est constituée d'un sous-ensemble d'organismes, connecté à d'autres sous-ensembles au sein du réseau généalogique du vivant, et délimité par deux événements de spéciation ou un événement de spéciation et un autre d'extinction » (Samadi & Barberousse 2006). La spéciation devient une division définitive du réseau généalogique.
En pratique, la définition de l'espèce a longtemps été confondue avec les critères utilisés pour la reconnaître et la délimiter. Tout critère permettant de montrer qu'un ensemble d'individus appartient à une communauté de reproduction ayant une histoire évolutive autonome est pertinent.
Les méthodes et la difficulté d'observation pouvant varier selon les espèces, il est normal de constater qu'aucun critère n'est satisfaisant pour tous les organismes. Plusieurs critères sont généralement utiles pour caractériser une nouvelle espèce.
Champignons, les quatre critères
Parmi tous les critères disponibles, quatre sont d'un intérêt particulier chez les champignons (Giraud et al., 2008) :
– Le critère biologique, basé sur l'observation de l'interfécondité. L'incompatibilité reproductrice (ou isolement reproducteur) de deux ensembles d'individus confirme qu'ils sont divergents. Mais en pratique, on peut parfois croiser au laboratoire certaines espèces de champignons et observer la production d'une descendance.
– Le critère phénétique, basé sur l'observation des ressemblances morphologiques héritables au sein d'un ensemble. La description des structures sexuées et asexuées est traditionnellement la base de la reconnaissance en mycologie.
– Le critère écologique, basé sur la capacité d'un ensemble d'individus à s'adapter à une niche écologique particulière. Très pertinent pour les champignons vu leur grande variabilité de styles de vie (parasitisme, saprophytisme ou symbiotisme).
– Le critère phylogénétique, basé sur la mesure de la divergence entre les séquences d'ADN des individus ; fort commode car universel et très discriminant.
C'est quoi, la sympatrie ?
Par ailleurs, plusieurs modes de spéciation sont observés chez les champignons. La spéciation est dite allopatrique lorsque les deux groupes se différencient dans des lieux séparés par des barrières géographiques (océans, montagnes), empêchant le flux de gènes entre les entités et entraînant donc l'isolement reproducteur.
À l'inverse, si l'isolement reproducteur est généré en l'absence de barrière évidente au flux de gènes et possiblement sur le même hôte, on parle de spéciation sympatrique (Giraud et al., 2008).
Ce mode de spéciation est relativement fréquent chez les champignons qui, en s'adaptant à des plantes hôtes spécifiques, finissent par isoler des populations distinctes pouvant cohabiter dans un même paysage.
Fig. 1 : Espèce : définition. D'après Samadi & Barberousse, 2006.
Les espèces sont indiquées dans des ensembles grisés. Les cercles représentent des individus et les traits les relations de parenté entre ces individus. Une espèce est délimitée dans le temps par un événement de spéciation (origine) et un événement d'extinction ou d'une nouvelle spéciation.
Fig. 2 : Critère phylogénétique pour définir B. pseudocinerea
Arbre du genre Botrytis montrant la position phylogénétique de la nouvelle espèce B. pseudocinerea et sa distinction d'avec B. cinerea. Noter la présence de B. fabae entre les deux.
Fig. 3 : Critère biologique, juin n'est pas septembre.
Évolution de la structure des populations de Botrytis sp. au cours du temps. B. pseudocinerea regroupe les clusters « I+ » et « I- ».
Fig. 4 : Critère biologique, suivi de la diversité.
Évolution de la proportion de clones dans les 3 clusters de Botrytis sp. au cours du temps.
La richesse clonale (G/N soit le nombre de combinaisons uniques d'allèles sur les 8 loci testés, par rapport au total des individus d'un cluster) mesure la proportion de clones différents dans un cluster et augmente avec elle (1 = diversité maximale).
2- Un peu d'histoire de Botrytis
Une phylogénie récente montre que le genre Botrytis (Ascomycota) est constitué de deux clades, l'un groupant des espèces capables de se développer sur des plantes mono- et dicotylédones, et l'autre sur des dicotylédones uniquement (Staats et al., 2005). Au sein de ce second clade, ce que l'on appelait jusqu'ici B. cinerea (tel. Botryotinia fuckeliana) présente le plus large spectre d'hôtes : au moins 220 espèces de plantes dont la vigne et des cultures légumières, fruitières et ornementales.
B. cinerea est très variable au niveau de sa morphologie et de sa diversité génétique. Ceci suggère de grandes tailles de population et une intense recombinaison génétique liée par exemple à la reproduction sexuée (Fournier & Giraud, 2008).
Depuis longtemps, les éléments transposables (i.e. des séquences d'ADN capables de se déplacer et se multiplier de manière autonome dans le génome) boty et flipper sont utilisés pour discriminer les individus de B. cinerea, nommés transposa s'ils en contiennent et vacuma s'ils n'en contiennent pas (Giraud et al., 1999). Ces marqueurs moléculaires, associés à des marqueurs microsatellites (Fournier et al., 2002) ont été à la base de la caractérisation, au sein de ce qu'on nommait auparavant B. cinerea, de deux espèces vivant en sympatrie (notion définie encadré 1) :
1) B. cinerea stricto sensu ou groupe II, espèce dominante dans les populations et contenant des souches transposa et des souches vacuma et
2) Botrytis groupe I, espèce minoritaire, supposée au début ne contenir que des souches de type vacuma (Fournier et al., 2005 ; Leroux et al., 2006).
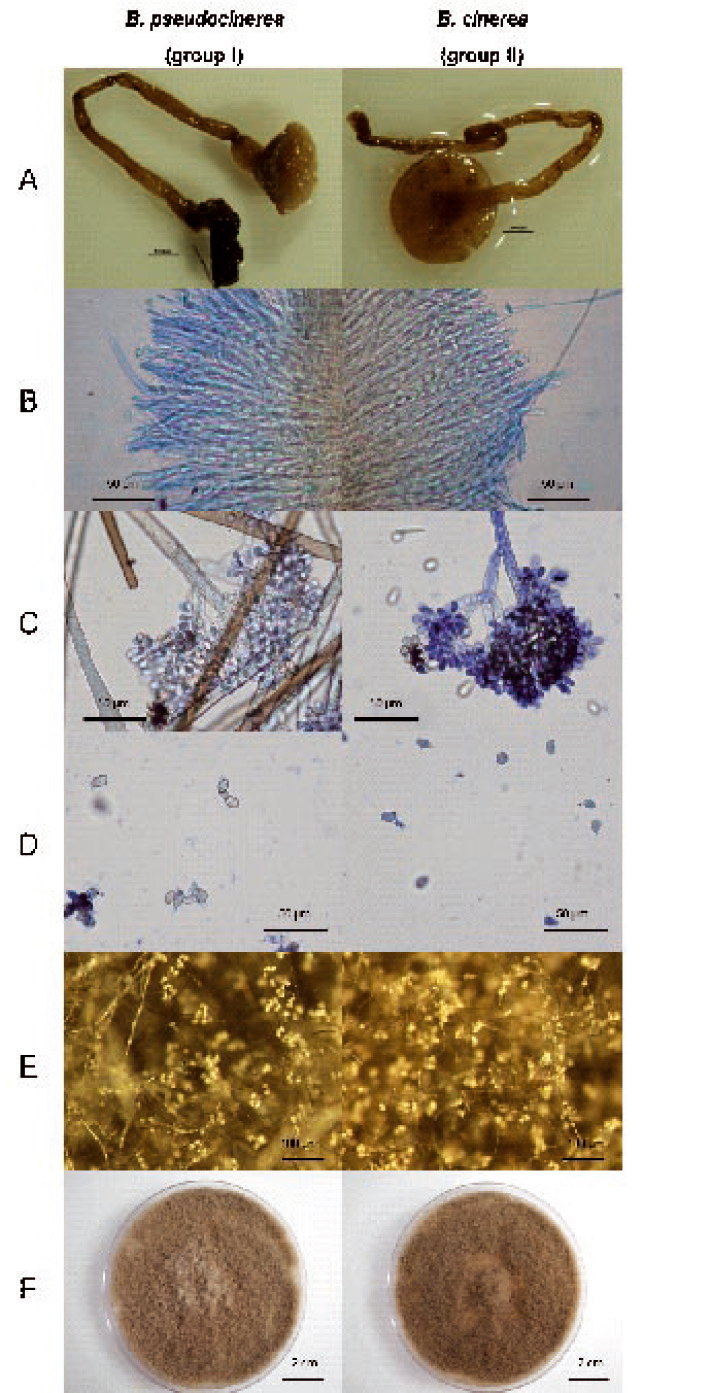
Fig. 5 : Critère phénétique, les Botrytis mis en miroir.
Caractéristiques morphologiques de Botrytis pseudocinerea (à gauche) et de Botrytis cinerea (à droite).
A : Apothécies, structures sexuées de Botrytis sp. ;
B : Asques, contenant les ascospores (spores sexuées), observées après dissection des apothécies ;
C : Conidiophores en arbuscule, portant les conidies ;
D : conidies (spores asexuées) ;
E : mycélium sporulant (10 jours) ;
F : culture de 10 jours sur milieu maltlevure.
Difficile de les différencier ainsi !
Observation des souches VD256 (B. pseudocinerea) et 1810 (B. cinerea). Coloration au bleu coton pour les observations microscopiques.

 Imprimer
Imprimer